Потеря зрения у пожилых людей является серьезной проблемой здравоохранения: примерно каждый третий человек к 65 годам страдает каким-либо заболеванием, снижающим зрение. Возрастная макулярная дегенерация (ВМД) является наиболее распространенной причиной слепоты в развитых странах. В Европе около 25% людей в возрасте 60 лет и старше имеют AMD. «Сухая» форма относительно распространена среди людей старше 65 лет и обычно вызывает только легкую потерю зрения. Однако примерно у 15% пациентов с сухой ВМД развивается более серьезная форма заболевания – экссудативная ВМД, или эксВМД, которая может привести к быстрой и необратимой потере зрения. К счастью, существуют методы лечения, которые могут замедлить дальнейшую потерю зрения. Несмотря на то, что в настоящее время не существует профилактических методов лечения, они изучаются в клинических испытаниях. Таким образом, период до развития exAMD может представлять собой критическое окно для терапевтических инноваций: можем ли мы предсказать, у каких пациентов будет прогрессировать exAMD, и помочь предотвратить потерю зрения еще до того, как она произойдет?
В нашей последней работе, опубликованной в журнале Nature Medicine, мы сотрудничали с глазной больницей Мурфилдс и Google Health, чтобы подготовить набор данных изображений сетчатки глаза, обучить систему искусственного интеллекта (ИИ), которая могла бы предсказывать развитие exAMD, и провести исследование для оцените нашу модель по сравнению с опытными клиницистами. Мы демонстрируем, что наша система способна работать так же хорошо или даже лучше, чем клиницисты, в прогнозировании того, будет ли глаз конверсировать в exAMD в следующие 6 месяцев. Наконец, мы исследуем потенциальную клиническую применимость нашей системы. Наш вклад подчеркивает потенциал использования ИИ в профилактических исследованиях таких заболеваний, как exAMD.
Набор данных AMD глазной больницы Мурфилдс
Мы использовали набор данных анонимных сканов сетчатки пациентов Moorfields с exAMD на одном глазу и с высоким риском развития exAMD на другом глазу. Это включает 2795 пациентов в семи различных центрах Мурфилдс в Лондоне с разным полом, возрастом и этнической принадлежностью. Эти пациенты регулярно посещают больницу для лечения, проходя трехмерную оптическую когерентную томографию (ОКТ) обоих глаз с высоким разрешением при каждом посещении. Часто существует задержка между развитием exAMD и его диагностикой и лечением. Чтобы решить эту проблему, мы работали с экспертами по сетчатке, чтобы просмотреть все сканы для каждого глаза и указать сканирование, когда exAMD впервые проявился.
Обучение системе раннего предупреждения для AMD
Наша система состоит из двух глубоких сверточных нейронных сетей, которые принимают в качестве входных данных многомерные объемные сканы глаз, где каждое сканирование состоит из 58 миллионов трехмерных пикселей (вокселей). В нашей предыдущей работе, которая теперь продолжается в сотрудничестве с Google Health, мы разработали модель, способную сегментировать эти сканы глаз на тринадцать анатомических категорий. Сегментированные данные были объединены с необработанным сканированием, и оба были использованы в качестве входных данных для модели прогнозирования, которая была обучена для оценки риска конверсии пациента в exAMD на другом глазу в течение следующих шести месяцев.
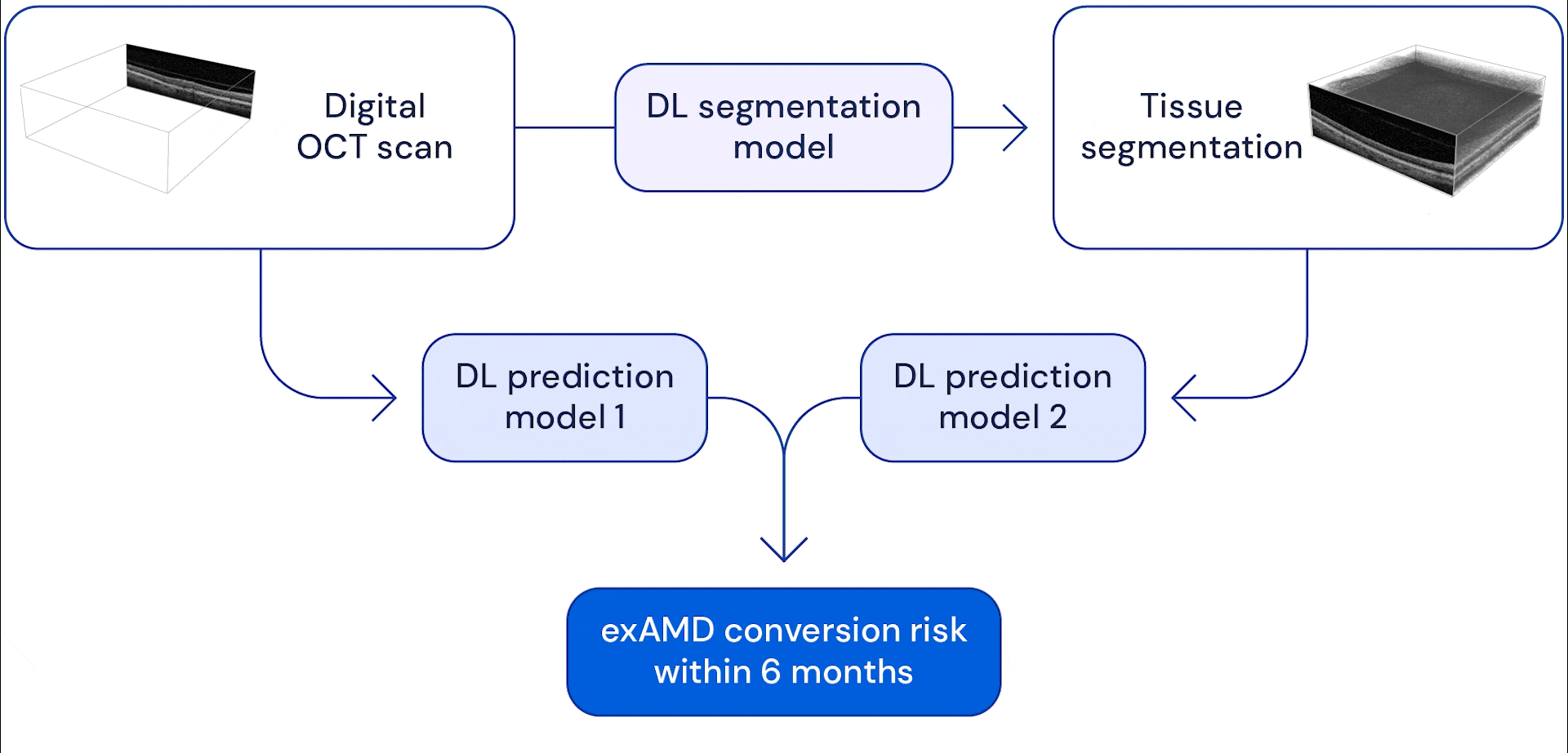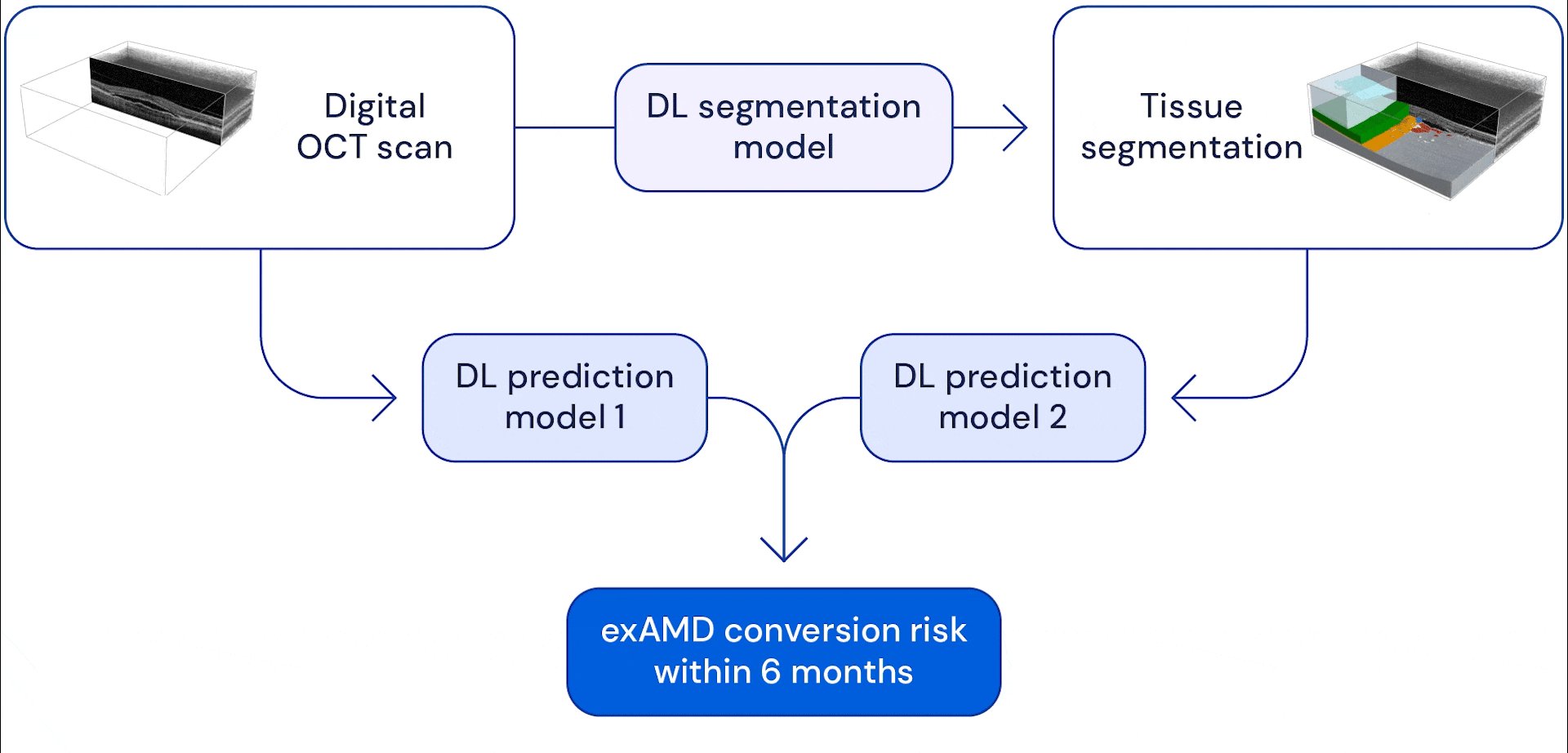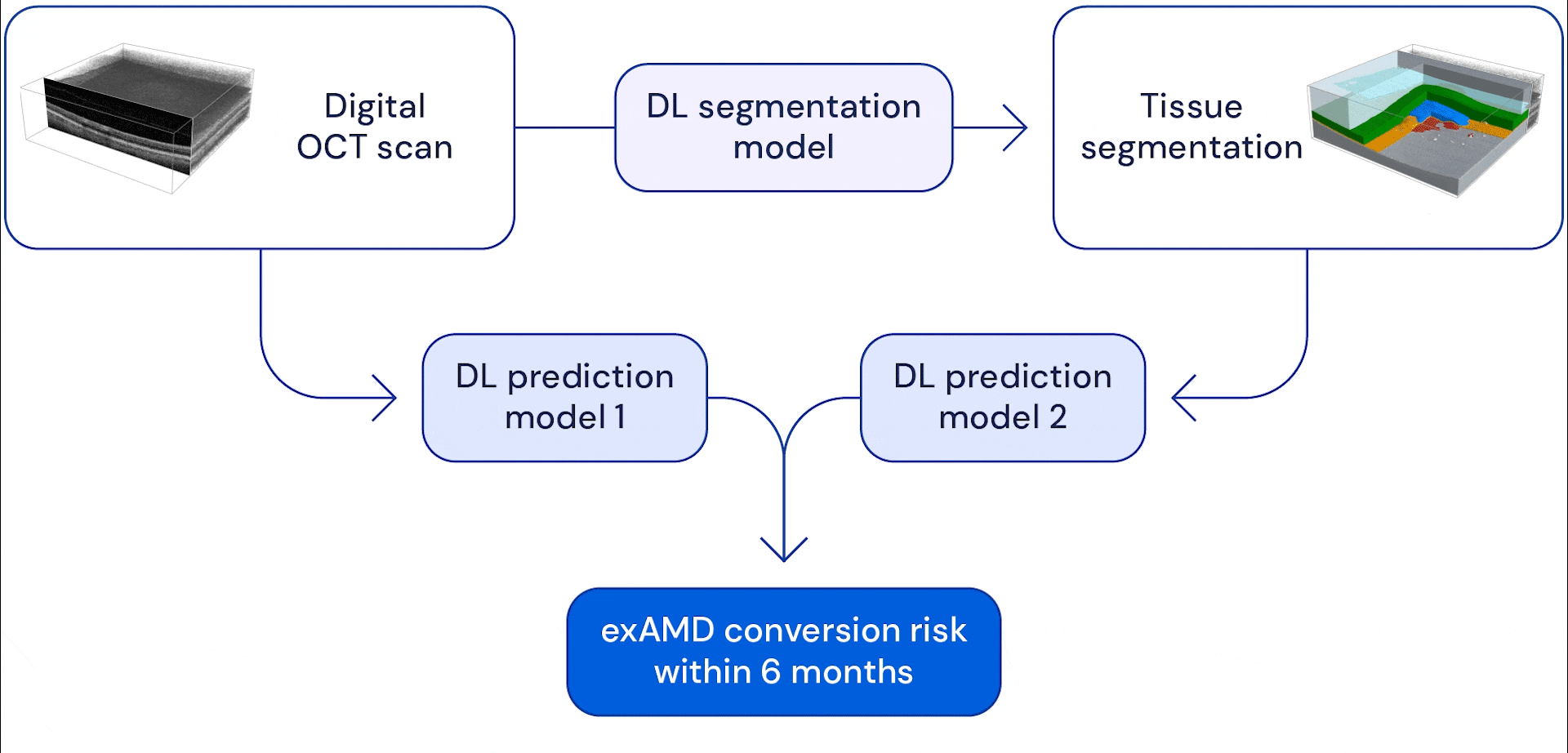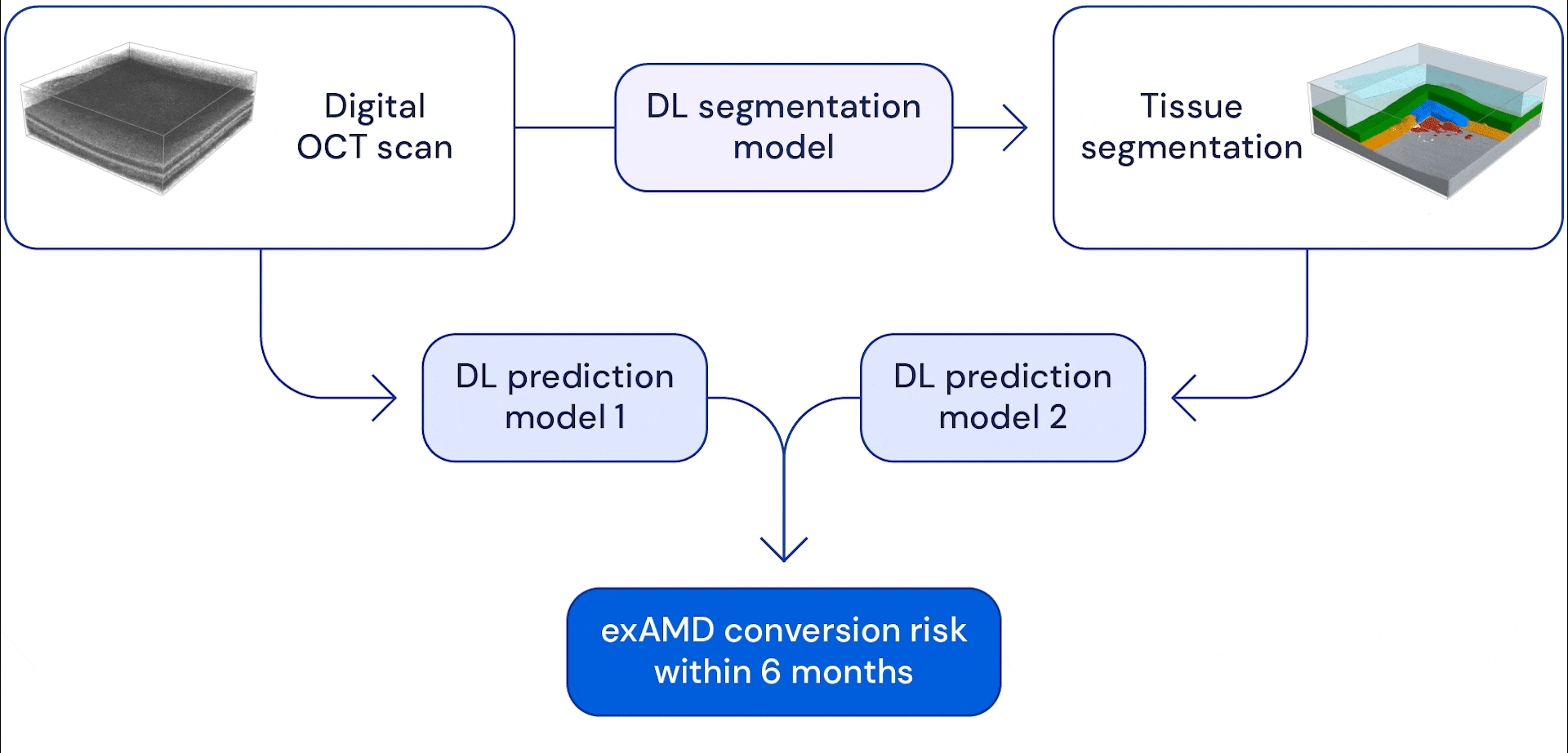
Преимущество двухэтапной системы заключается в том, что она дает ИИ разные виды сканирования глаз. Анатомическая сегментация изображений помогает системе научиться моделировать риски на основе признаков известных анатомических показателей, таких как друзы (небольшие жировые отложения) или потеря пигментного эпителия сетчатки (который помогает питать и защищать другие слои сетчатки). Предоставление необработанных сканов глаз позволяет модели научиться замечать другие тонкие изменения, которые могут стать потенциальными факторами риска. В конце система объединяет информацию, которую она извлекает из этих сканирований, чтобы предсказать, когда и будет ли глаз прогрессировать до exAMD в течение следующих 6 месяцев. Мы выбрали это временное окно, чтобы система могла заранее предсказать как минимум два интервала наблюдения, предполагая, что максимальный интервал наблюдения составляет 3 месяца.
Клинический экспертный эталон для предсказания будущего
Важно установить эталон производительности человека, чтобы сравнить, насколько хорошо наша система работает в соответствии с клиническими стандартами. Однако прогнозирование exAMD не является рутинной задачей, выполняемой клиницистами, поэтому неясно, возможна ли вообще эта задача. Чтобы выяснить это, мы провели исследование с шестью экспертами по сетчатке — тремя офтальмологами и тремя оптометристами, каждый из которых имеет не менее десяти лет опыта, — чтобы предсказать, будет ли глаз трансформироваться в exAMD в течение следующих 6 месяцев. Несмотря на новизну задачи, эксперты справились лучше, чем случайность, однако задача сложная, и их оценки существенно разошлись. Наша система работала так же, а в некоторых случаях и лучше, чем эксперты, в прогнозировании прогрессирования exAMD, в то же время демонстрируя меньшую вариабельность в согласии с каждым экспертом по сравнению с экспертами друг с другом.
ВМД — невероятно сложное заболевание, серьезно влияющее на жизнь миллионов людей во всем мире. С помощью этой работы мы не решили проблемы AMD… но я думаю, что мы просто добавили еще один большой кусок головоломки.
Пирс Кин, ученый-клиницист NIHR
Визуализация прогрессирования заболевания
Для системы может быть недостаточно просто предоставить прогноз: клиницисты также могут в идеале искать информацию об анатомической основе для прогнозов, которая может быть существенно полезной для дальнейшей интерпретации (например, для планирования исследований или рассмотрения лечения). Преимущество нашей системы заключается в том, что она автоматически сегментирует каждое сканирование на известные типы тканей. Извлечение этих анатомических и патологических особенностей обеспечивает систематический метод визуализации изменений в этих тканях с течением времени. Показатели риска, полученные нашей системой, соответствуют анатомическим изменениям с течением времени и вместе дают более полную картину конверсии exAMD.

Предвидение важнее задним числом
Мы воодушевлены потенциалом поддержки клиницистов и исследователей путем разработки систем, которые могут помочь выявлять заболевания сетчатки на более ранних этапах и информировать клиническое понимание их прогрессирования. Система прогнозирования, подобная этой, может использоваться для информирования о соответствующих интервалах наблюдения для эффективного лечения пациентов с высоким риском. Наша работа основана на многообещающих ранних работах по разработке прогностических моделей для exAMD на основе фотографий сетчатки и ОКТ-сканов. С момента начала нашего сотрудничества с глазной больницей Мурфилдс в 2016 году мы опубликовали два многообещающих исследования, в которых подчеркивается потенциал ИИ для преобразования здравоохранения сетчатки.
Однако мы знаем, что еще многое предстоит сделать – эта работа еще не представляет собой продукт, который можно было бы внедрить в рутинную клиническую практику. Хотя наша модель может делать прогнозы лучше, чем клинические эксперты, есть много других факторов, которые необходимо учитывать, чтобы такие системы были эффективными в клинических условиях. Хотя модель была обучена и оценена на репрезентативной популяции крупнейшей глазной больницы в Европе, потребуется дополнительная работа для оценки эффективности в контексте очень разных демографических данных. Недавнее исследование, посвященное использованию другой системы искусственного интеллекта в клинических условиях, выявило лишь некоторые социотехнические проблемы для таких систем на практике. Еще один момент, с которым трудно спорить, заключается в том, что любая система прогнозирования будет иметь определенный уровень ложных срабатываний: то есть, когда у пациента обнаруживается состояние или прогнозируется его развитие, которого на самом деле у него нет. Компромисс, связанный с добавлением неточной системы искусственного интеллекта в цикл раннего предупреждения, может быть излишне дорогостоящим для пациентов, которые на самом деле не подвержены риску, и его необходимо тщательно учитывать в клинических исследованиях того, как такие системы могут использоваться на практике. В этой статье мы предлагаем две рабочие точки системы, чтобы сбалансировать чувствительность (показатель того, насколько хорошо она правильно идентифицирует заболевание) и специфичность (показатель того, насколько низок уровень ложноположительных результатов). Например, при специфичности 90% достигается чувствительность 34%, что означает, что система правильно определила прогрессирование в одной трети сканирований, которые действительно прогрессировали в течение 6 месяцев. Это могло бы определить количество пациентов с высоким риском с точностью, которая может быть достаточной для изучения новых стратегий лечения, которые могут уменьшить потерю зрения и улучшить результаты лечения пациентов.
Мы хотели бы поблагодарить офтальмологическую больницу Мурфилдс и клиницистов, которые помогали собирать данные и участвовали в нашем сравнительном исследовании. Пожалуйста, смотрите документ для всех благодарностей и более подробной информации о работе. Кроме того, мы открыли исходный код модели для будущих исследований, доступный здесь, и Мурфилдс сделает набор данных доступным через Инициативу Райана по исследованию желтого пятна.
